بحث عن الروابط التساهمية
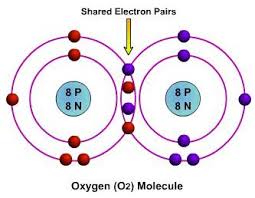
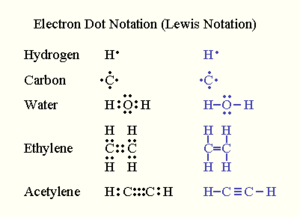
وقد قام باقتراح ما يسمى ببناء لويس أو الشكل الإلكتروني النقطي والذي يكون.
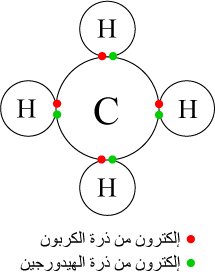
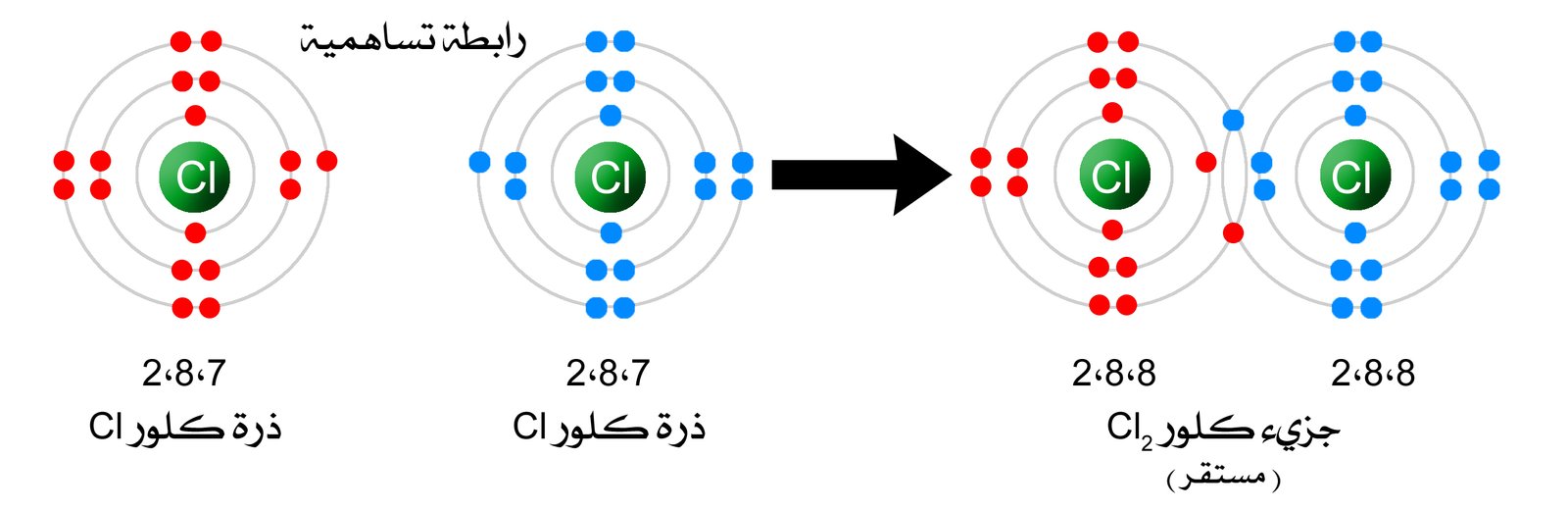
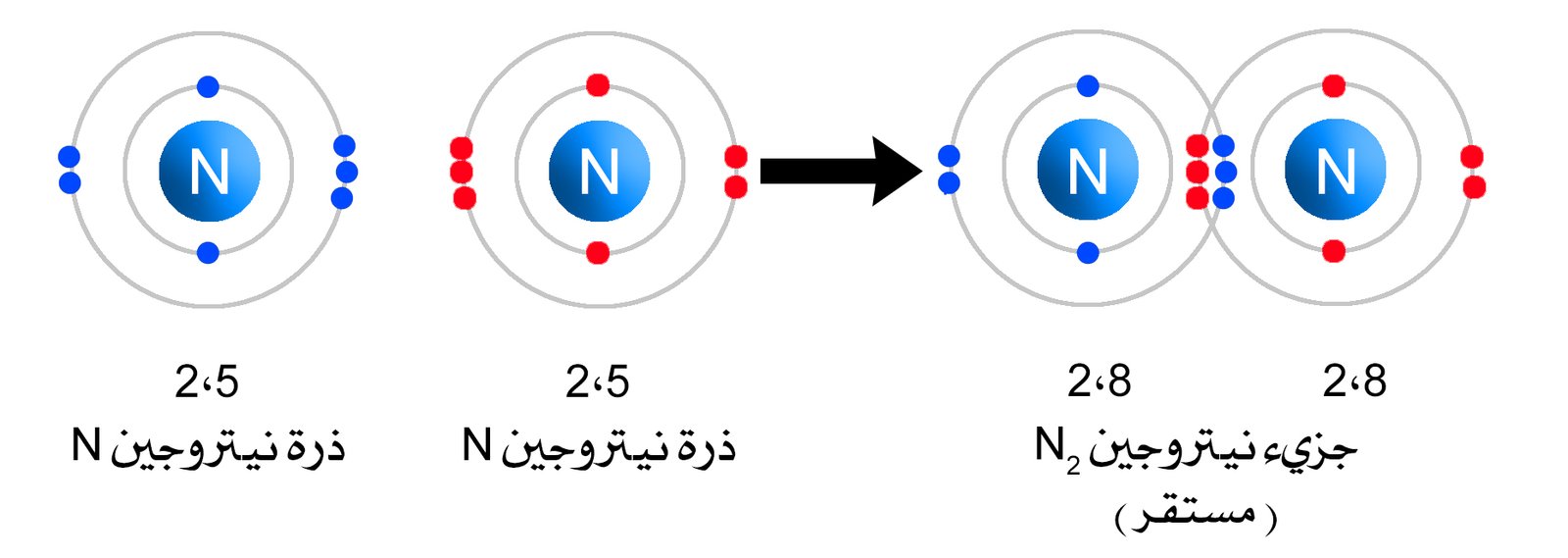
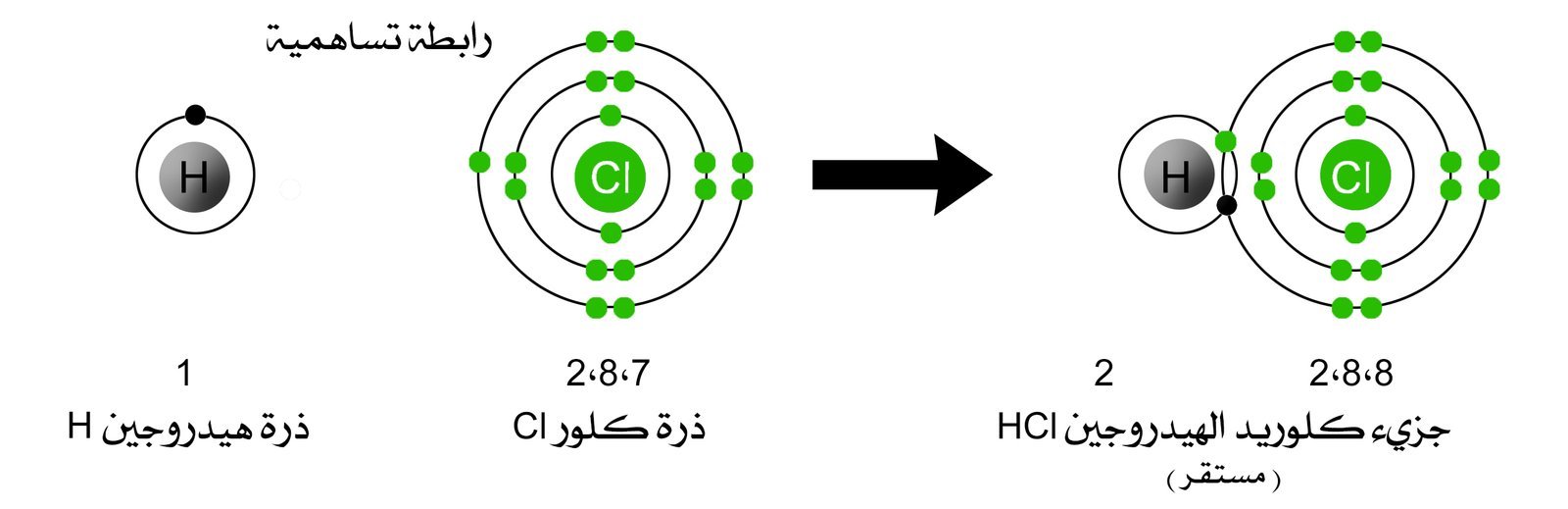
بحث عن الروابط التساهمية. تميل الذرات للمساهمة أو المشاركة بإلكتروناتها بالطريقة. سنقدم إليكم اليوم بحث عن الرابطة التساهمية والروابط التساهمية هي احد الروابط الكيميائية ويتم فيها ارتبط بين زوج أو اكثر من الإلكترونات يزيد من قوة الجزيء وتتم الروابط التساهمية في الجزيئات التي تتكون ذراتها من. أم ا الرابطة التساهمية فليست برابطة ضعيفة بل هي رابطة أقوى من الرابطة الأي ونية الواحدة بالطبع لسبب بسيط وهو أن الرابطة الأي ونية عبارة عن تجاذب كهربي أي أنه ليس لها وجود مادي فهي مجرد طاقة بينما الرابطة التساهمية. بحث ـ تقرير جاهز عن الروابط الكيميائية doc pdf أنواع الروابط الكيميائية مثال مع الحل مسائل تمارين أمثلة على الروابط الكيميائية كتب ومراجع وبحوث في الكيمياء بروابط تحميل مباشرة مجانا وقراءة أونلاين.
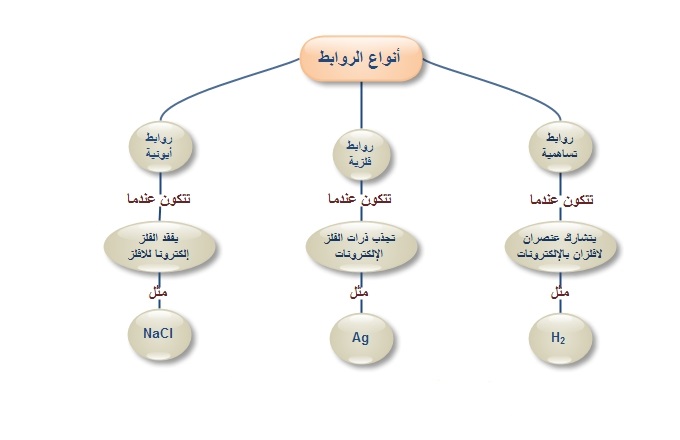
الفلز هو ذلك العنصر الكيميائي ال ذي يكو ن أيونات موجبة عندما يفقد الإلكترونات وتوجد رابطة بين ذراته تسمى الرابطة الفلزية والروابط الفلزية هي عبارة عن روابط كيميائي ة تحدث بين عنصرين من. الرابطة التساهمية هى أحد أشكال الترابط الكيميائي وتتميز بمساهمة زوج أو أكثر من الإلكترونات بين الذرات مما ينتج عنه تجاذب جانبي يعمل على تماسك الجزيء الناتج. في بحث عن الروابط التساهمية نجد أنها تنقسم إلى نوعان هما الروابط التساهمية القطبية والغير قطبية ولا يختلفان عن بعضهما كثيرا و تتمثلان في وجود قوتا تجاذب أحدهما أكبر من الأخرى مثل أن يقوم طرف قوي بجذب شيء بقوة أكبر من. الرابطة التساهمية هي الرابطة التي تنشأ عن مشاركة الالكترونات والجزيئ هو أصغر وحدة في المركب ويتكون الجزيئ عندما ترتبط ذرتان أو أكثر بروابط تساهمية وتعد الالكترونات المشتركة جزءا من الكترونات مجال الطاقة.